5月29日,据药物临床试验登记与信息公示平台显示,赛诺菲登记了一项Riliprubart注射液的Ⅲ期临床试验,针对慢性炎性脱髓鞘性多发性神经根神经病。据公开资料显示,Riliprubart(BIVV020/SAR445088)是一款补体C1s单抗。

图片来源:药物临床试验登记与信息公示平台
针对CIDP
海外Ⅲ期进行中
慢性炎性脱髓鞘性多发性神经根神经病(CIDP)主要由免疫抗体介导反应引起,是一种较为罕见的严重感觉运动障碍周围神经病变,患病率约为1/10000~9/10000。据了解,CIDP病情表现严重,包括四肢瘫痪、呼吸衰竭甚至死亡,同时还可能伴有神经内膜的间质和血管周围炎性T细胞和巨噬细胞浸润等症状。
补体C1s作为补体系统中的重要成分之一,在炎症反应和清除病原体中发挥着关键作用,C1s蛋白参与了补体级联反应的启动过程。相关研究显示,补过度激活体系统可能导致组织损伤和疾病发生,因此,阻断C1s蛋白的功能有望治疗多种自身免疫性疾病。
Riliprubart是赛诺菲开发的一款补体C1s单抗,能够通过阻止补体系统的过度激活,从而减轻CIDP患者的炎症反应。2023年11月,Riliprubart被CDE纳入突破性治疗品种,用于治疗CIDP。
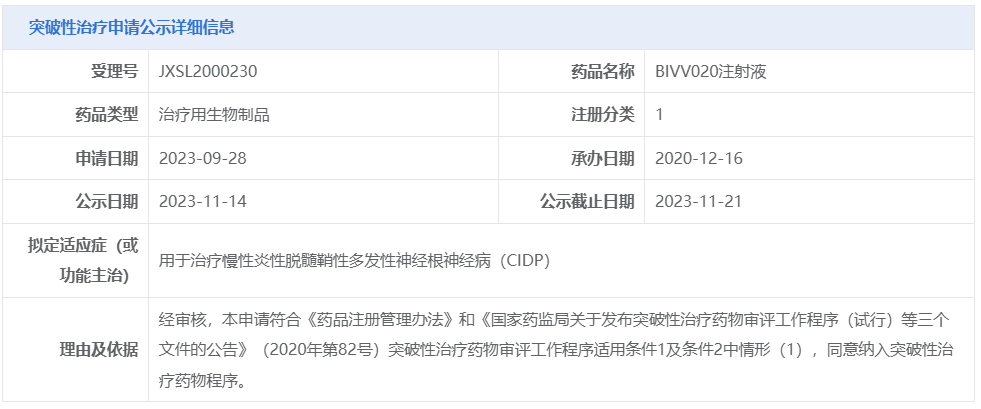
图片来源:CDE官网
目前,赛诺菲正在海外进行Ⅲ期临床研究;今年3月,赛诺菲在美国神经病学会年会(AAN)上公布了Riliprubart治疗CIDP的II期研究数据。本次赛诺菲在国内登记的试验,是一项在难治性CIDP受试者中评价 Riliprubart 的疗效和安全性的 Ⅲ 期、双盲、安慰剂对照研究。
聚焦自免领域
加速管线拓展
免疫学和炎症(I&I)是赛诺菲重点布局的研究领域,多款产品展现出了巨大潜力,包括“百亿爆款”Dupixent、全球首个抗IL-6单抗“Kevzara”等。
除Riliprubart外,赛诺菲另有一款补体C1s单抗“Sutimlimab”已获批上市。此外,近期赛诺菲I&I管线上有多个项目取得了重要进展。
Sutimlimab
Sutimlimab于2022年2月获美国FDA批准上市,用于冷凝集素病(CAD)患者降低由于溶血导致的红细胞输注需求。与Riliprubart作用机理类似,Sutimlimab通过阻断经典补体途径中C1s蛋白的功能而发挥抑制溶血的作用。据了解,作为FDA批准的首款用于治疗CAD的补体C1s抗体,Sutimlimab在上市首个完整年实现了0.72亿欧元销售额,同比上涨240.9%。
Rilzabrutinib
Rilzabrutinib是一款BTK抑制剂,目前正被研究用于治疗天疱疮、免疫性血小板减少症(ITP)、慢性自发性荨麻疹(CSU)等自身免疫性疾病。近日,赛诺菲公布了Rilzabrutinib的一项Ⅱ期研究的积极结果,数据显示该药物可使中度至重度哮喘患者发生哮喘失控(LOAC)的事件数量减少,同时改善未控制的症状。
Frexalimab
Frexalimab是一款CD40L单抗,于2024年4月在华获批临床。日前,赛诺菲在药物临床试验登记与信息公示平台上登记了该药物的一项临床试验,针对的是非复发性继发进展型多发性硬化(nrSPMS)成人受试者。据2024年2月刊登于《新英格兰医学杂志》上的一项研究显示,Frexalimab能够显著减缓复发性硬化患者的疾病活动。
此外,赛诺菲I&I管线上还有多款药物正持续推进临床研究,包括OX40L靶向单抗Amlitelimab、IL-13/TSLP双重阻断剂Lunsekimig等。
结语
基于自免疾病庞大的市场规模以及未满足临床需求,通过加速自免等领域的在研管线研究进度,赛诺菲有望取得更进一步的创新成果。







