今日,Seres Therapeutics宣布,该公司开发的微生物组疗法SER-109,在治疗复发性艰难梭菌感染(CDI)的关键3期临床试验ECOSPOR III中获得积极顶线结果。该研究显示,与安慰剂相比,SER-109导致给药8周内CDI出现复发的患者比例显著下降,疗效结果超过之前与美国FDA协商确定的阈值。Seres计划依据这一临床结果,向美国FDA递交监管申请。4年前,SER-109在治疗CDI的2期临床试验中未能展现出显著疗效,然而在研究人员的不懈努力之下,它在关键性3期临床试验中最终获得了成功。

艰难梭菌感染(CDI)是美国最紧急的三大抗生素耐药性细菌威胁之一,也是美国医院获得性感染的主要原因。CDI与衰弱性腹泻相关,它显著影响患者的生活质量。自从四十多年前发现艰难梭菌以来,万古霉素一直是患者管理最常用的药物。然而,目前的治疗方法仍然留下了大量疾病复发的患者。
SER-109是一种研究性、口服、生物源性微生物组治疗药物,旨在减少CDI的复发,使患者通过打破CDI复发的恶性循环,恢复胃肠道微生物组的多样性,达到持续的临床缓解。SER-109由多种厚壁菌门菌种的纯化细菌孢子组成。FDA已授予SER-109突破性疗法认定和孤儿药资格,用于治疗CDI。
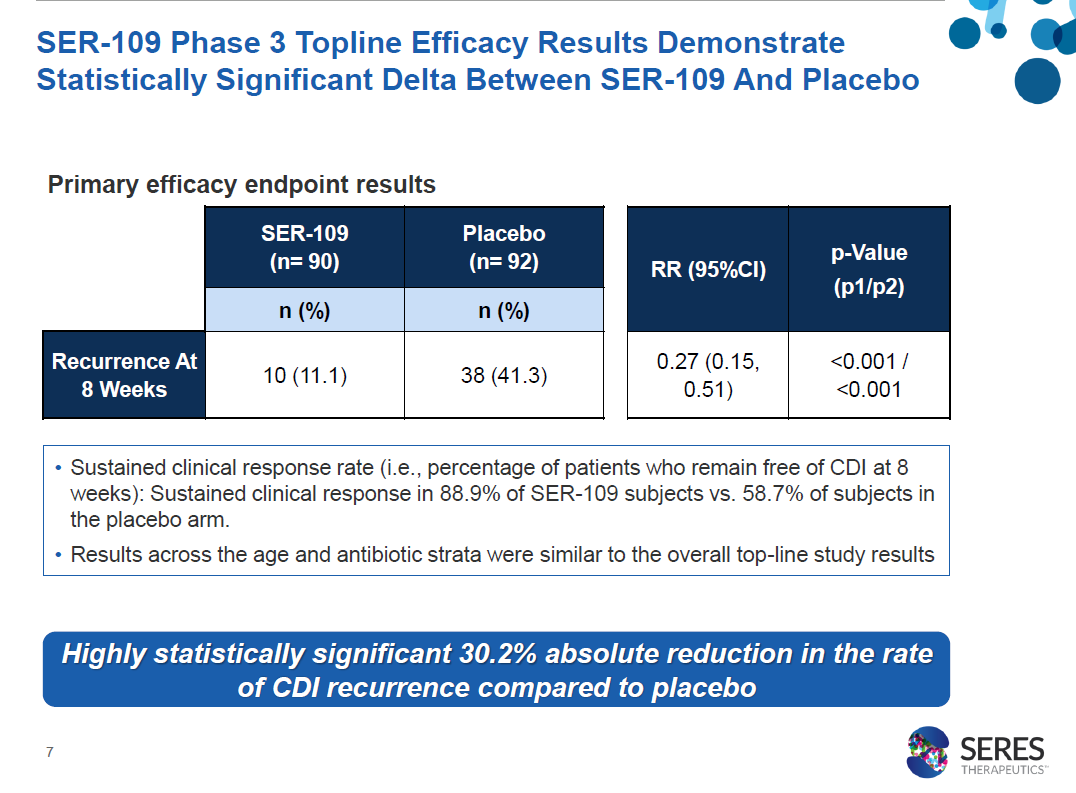
在SER-109试验中,182名复发型CDI患者接受了SER-109或安慰剂的治疗,所有患者同时接受标准抗生素治疗。试验结果表明,SER-109达到试验的主要终点,接受治疗8周后,SER-109组患者的复发率为11.1%,而安慰剂患者为41.3%。与安慰剂组相比,SER-109治疗组的相对风险为0.27(95% CI=0.15~0.51)。