8月12日,中国国家药监局药品审评中心(CDE)公示,礼进生物提交1类生物新药LVGN6051单克隆抗体注射液的临床试验申请,并获得受理。这是一款CD137激动抗体,目前正在美国开展1期临床试验。此前,该产品已与默沙东(MSD)的PD-1抑制剂Keytruda达成联合用药合作,以评估组合用药治疗多种恶性肿瘤的效果。

截图来源:CDE官网
CD137是肿瘤坏死因子(TNF)受体家族的成员,又称TNFRSF9或者4-1BB,由淋巴细胞激活(ILA)诱导,是共刺激免疫检查点分子。它可以由激活后的T细胞表达,而且在CD8 T细胞上的表达量比在CD4 T细胞上的表达量更高。CD137最具特征的功能是其对T细胞的共刺激活化作用。它的交联可增强T细胞增殖,IL-2分泌,存活和细胞溶解活性。此外,CD137可以增强免疫活性以消除小鼠中的肿瘤。
根据礼进生物官网介绍,给药后,LVGN6051结合并激活在各种白细胞亚群上表达的CD137,包括活化的T淋巴细胞和自然杀伤(NK)细胞。这增强了CD137介导的信号传导,诱导了细胞因子的产生,并促进了T细胞介导的抗肿瘤免疫反应。与已进入临床的第一代CD137激动性抗体不同,LVGN6051有选择性地在肿瘤微环境中局部激活CD137,减少正常组织免疫副反应。

▲LVGN6051作用机理(截图来源:礼进生物官网)
今年6月,礼进生物宣布与默沙东旗下子公司达成临床试验合作协议,以评估LVGN6051与默沙东的PD-1抑制剂可瑞达(Keytruda,帕博利珠单抗)治疗多种恶性肿瘤中的效果,包括肺癌、黑色素瘤、错配修复缺陷(dMMR)或高微卫星不稳定(MSI-H)的胃肠道癌和淋巴瘤。
目前,礼进生物正在美国进行LVGN6051单独使用或与抗PD-1抗体联合使用的1期临床试验。此次是该产品首次在中国申报临床试验并获受理,该公司计划在2021年第一季度正式在中国启动1期临床试验。
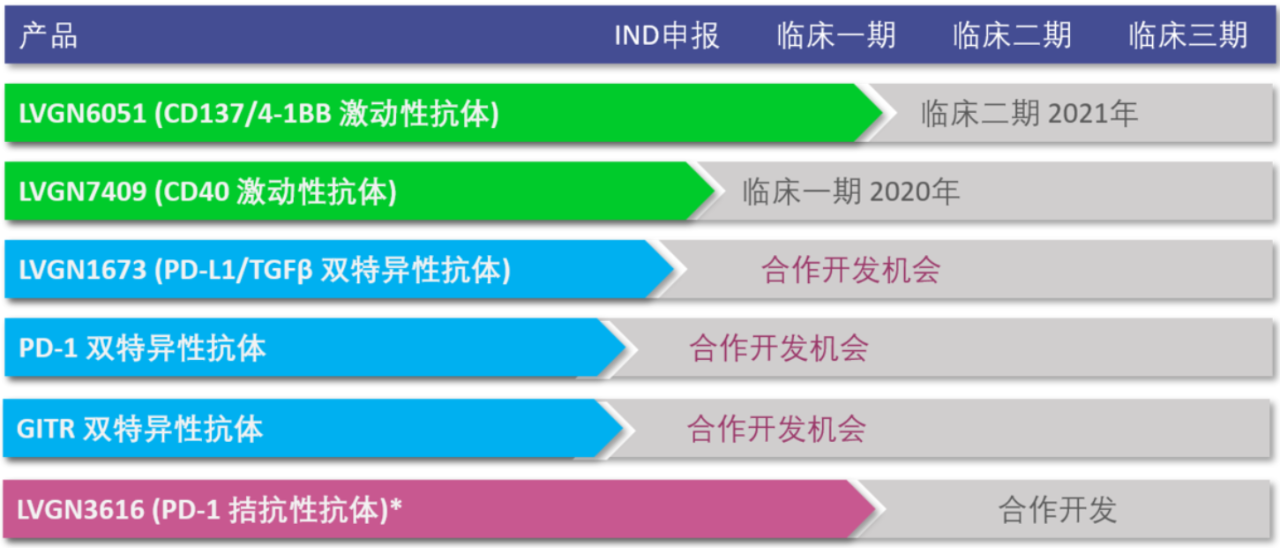
▲礼进生物在研管线(截图来源:礼进生物官网)
礼进生物由王结义博士于2016年创立,以其全球创新的肿瘤免疫激动性抗体管线为核心。目前,其在研管线已经有6款创新候选药。其中,针对 CD40靶点的激动性抗体LVGN7409已在临床申报准备阶段。







