7月9日,CDE官网显示,信诺维医药的注射用亚胺培南西司他丁钠福诺巴坦(简称注射用亚胺西福)上市申请获正式受理。这款全球首创的抗菌新药拟用于治疗医院获得性细菌性肺炎和呼吸机相关性细菌性肺炎(HABP/VABP),直击当前临床最棘手的耐药菌感染难题。
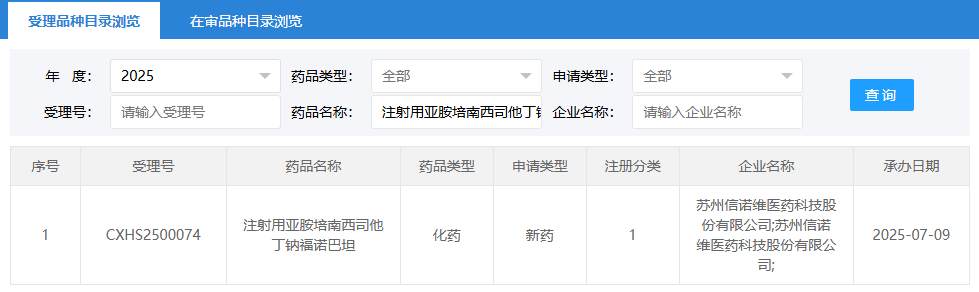
图片来源:CDE官网
与其他新型β-内酰胺酶抑制剂(如阿维巴坦、瑞莱巴坦等)相比,该产品具有更广、更强的抑酶活性,能全面有效抑制革兰阴性菌常见的A、C、D类酶活性。
这一突破性进展背后,是一家成立仅8年的中国药企在耐药菌战场上的关键突围。
在重症监护病房里,医院获得性肺炎和呼吸机相关肺炎是危及生命的常见感染。而更令人担忧的是,碳青霉烯类耐药革兰阴性杆菌的检出率持续走高,使得传统“最后一道防线”抗生素逐渐失效。
世界卫生组织(WHO)早已将对碳青霉烯耐药的鲍曼不动杆菌(CRAB)、铜绿假单胞菌(CRPA)和肠杆菌(CRE)列为三大具有严重威胁的耐药菌。 这些耐药菌导致的感染死亡率极高,临床治疗选择极为有限。
信诺维此次申报上市的亚胺西福,正是瞄准这一重大未满足临床需求。作为一款新型β-内酰胺类/β-内酰胺酶抑制剂复方制剂,它能同时有效对抗三大碳青霉烯耐药革兰阴性杆菌,成为全球首款具有如此广谱抗菌活性的BL/BLI药物。
此次申报基于XNW4107-302国际多中心III期临床研究(Reitab Study)的积极结果。这项前瞻性、双盲、随机、阳性药物对照的关键研究,覆盖全球多个研究中心,共入组449例患者。
研究结果显示,在主要终点——第14天全因死亡率方面,亚胺西福达到了非劣效性结果。更为重要的是,在临床治疗成功率和耐药菌微生物清除率方面,该药物表现出比对照组更优异的结果。

图片来源:药智数据企业版——全球临床试验
信诺维医药这家成立于2017年的创新药企,近年来在行业内动作频频。
就在5月29日,信诺维宣布与日本安斯泰来达成一项独家许可协议,将其靶向CLDN18.2的新一代抗体偶联药物XNW27011的海外权益授予安斯泰来。该交易总金额超过105亿人民币,成为今年中国创新药出海的重要案例之一,根据协议,信诺维将获得 9.35 亿人民币首付款。
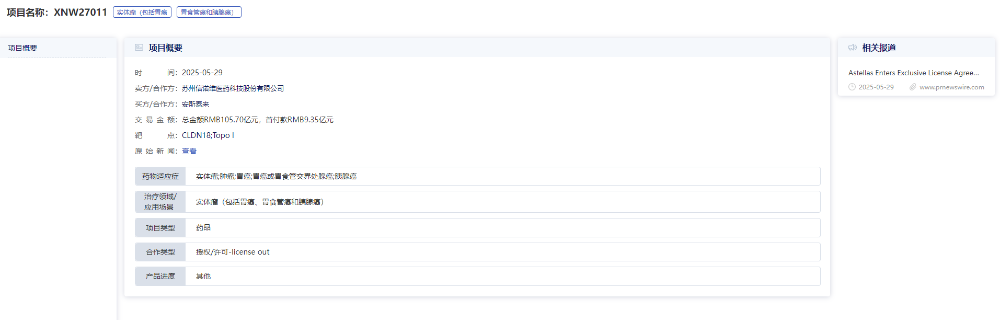
图片来源:药智数据企业版——投资格局
去年2月,信诺维成功完成了7亿元的E轮系列融资。融资由腾讯投资和国鑫投资联合领投,多家知名机构共同参与,老股东正心谷资本持续支持。
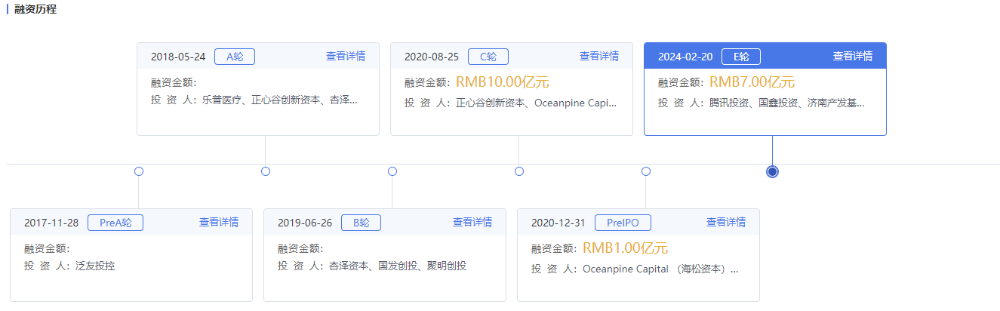
图片来源:药智数据企业版——投资格局
目前公司已有10个产品处于临床研发阶段,覆盖肿瘤精准治疗、多重耐药菌感染和代谢性疾病三大领域。







