作为关键的免疫检查点,程序性死亡配体1(PD-L1)通过与其受体-细胞膜上的程序性细胞死亡蛋白1(PD-1)相互作用来抑制抗肿瘤免疫。阻断PD-L1/PD-1相互作用可显著增强抗肿瘤免疫应答,是癌症治疗的重大突破。但核PD-L1(nPD-L1)的功能和易位机制目前尚不明确。
Caspase-1、-4、-5或-11切割Gasdermin D(GSDMD)是典型的焦亡通路。最近的研究表明,选择性地将活性的Gasdermin蛋白运送到癌细胞或在癌细胞中对Gasdermin B(GSDMB)和GSDME进行颗粒酶导向的切割可以诱导强大的抗肿瘤免疫,提示我们可通过诱导肿瘤细胞焦亡来进行抗癌治疗。
2020年9月14号,美国德克萨斯大学安德森癌症中心的洪明奇(Mien-Chie Hung)课题组在Nature Cell Biology发表了题为PD-L1-mediated gasdermin C expression switches apoptosis topyroptosis in cancer cells and facilitates tumour necrosis的研究论文,该研究首次发现nPD-L1 / GSDMC / caspase-8介导癌细胞焦亡,从而导致肿瘤坏死。

DOI:10.1038/s41556-020-0575-z
为了研究nPD-L1的生理作用,研究人员筛选了可能影响nPD-L1在MDA-MB-231细胞中表达水平的刺激物,包括应激,自噬,细胞因子,临床药物和PD-L1抗体。结果表明,低氧处理72小时可诱导大量的PD-L1分子进入细胞核。
随后,研究人员检测MDA-MB-231细胞中p-Y705-Stat3与PD-L1之间是否有相互作用。发现p-Y705-Stat3与PD-L1发生物理相互作用,并且该相互作用需要PD-L1的胞内结构域参与。并且,Stat3-Y705F突变体稳定表达的细胞中,PD-L1的核易位明显受损。尽管PD-L1和p-Y705-Stat3在胞质相互结合,但用importin α和β抑制剂伊维菌素处理可以抑制PD-L1核转位。
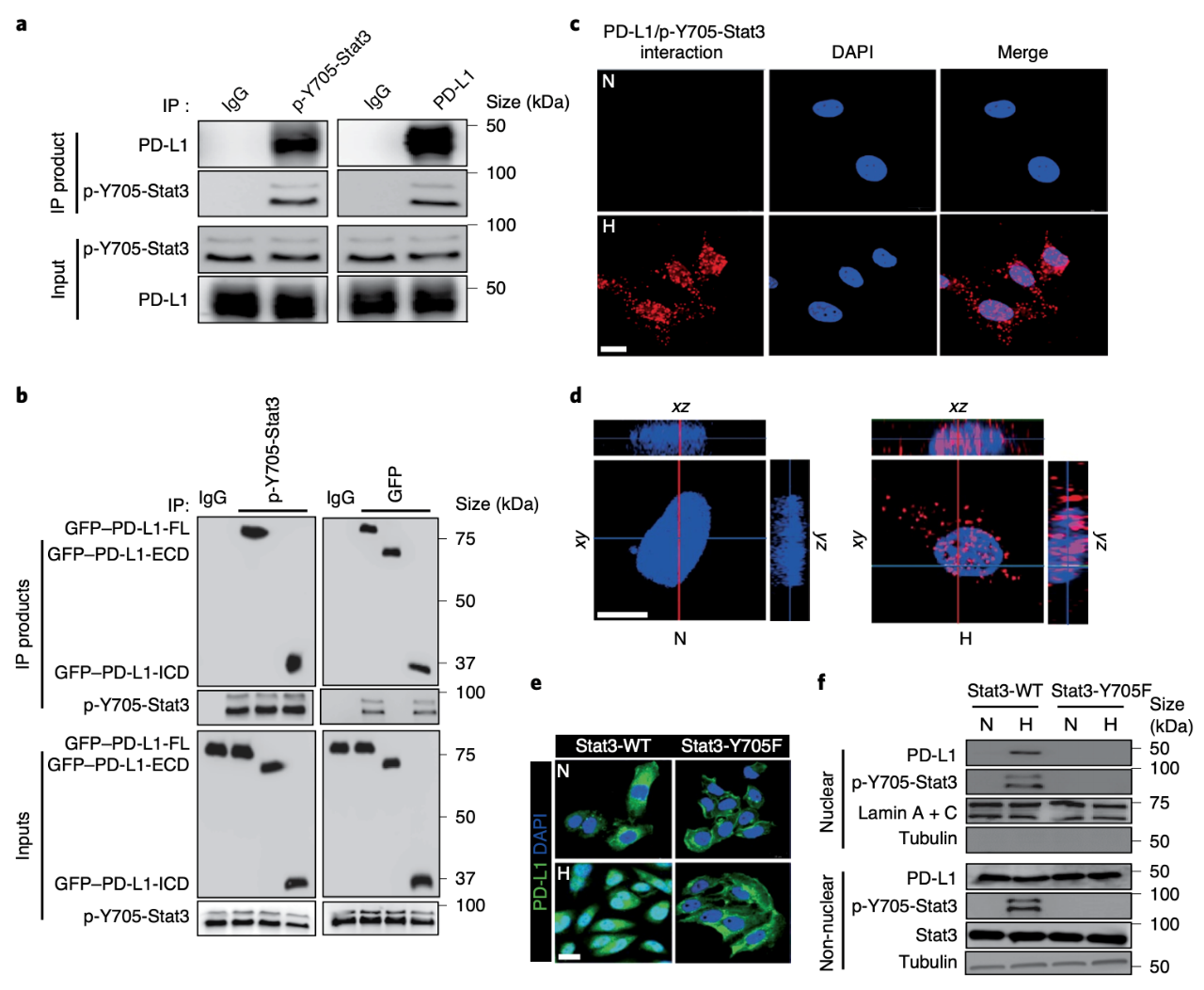
MDA-MB-231细胞中的PD-L1 / P-Y705-Stat3相互作用
接下来,研究人员发现,包括肺癌,乳腺癌,肝癌和卵巢癌以及黑色素瘤在内的多种癌细胞均可发生细胞焦亡,抑制磷酸化的Stat3可以有效的阻止PD-L1入核。另外,在缺氧条件下,在肿瘤细胞中nPD-L1将TNFα诱导的焦亡切换为焦磷酸化。
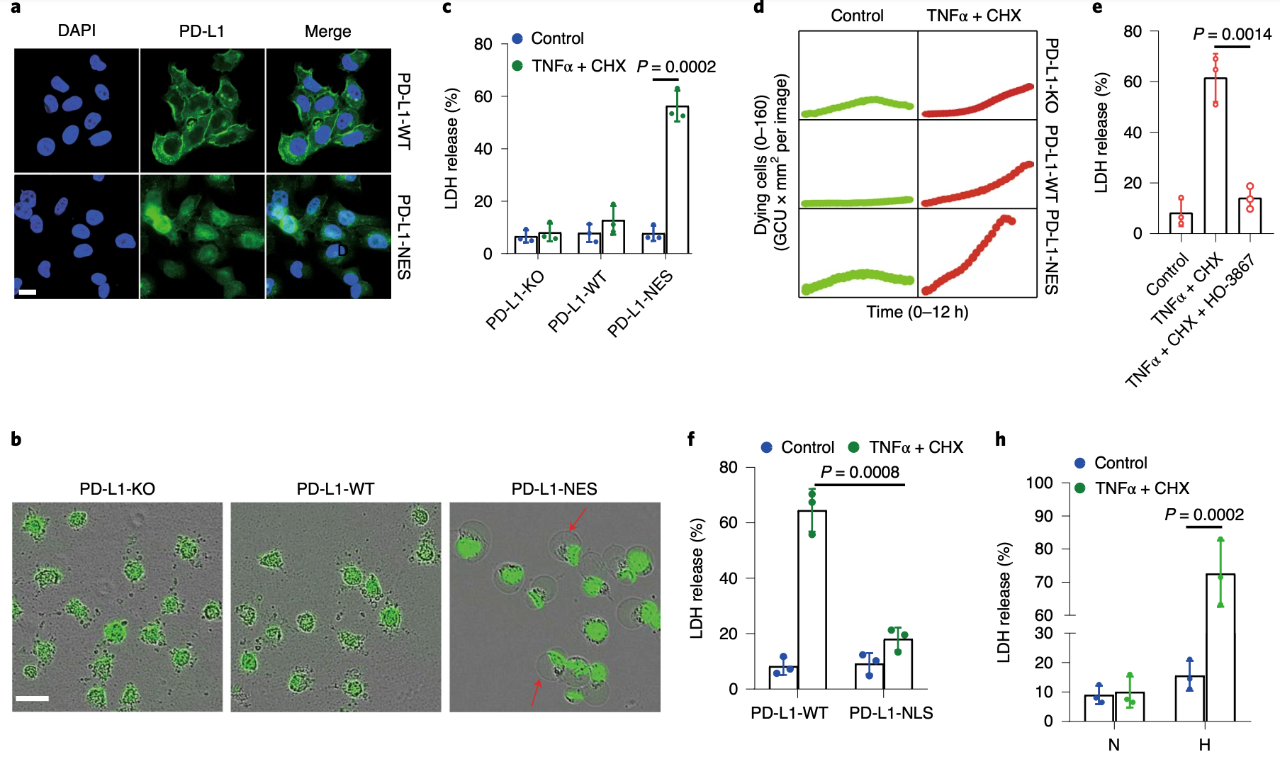
MDA-MB-231细胞中的PD-L1 / P-Y705-Stat3相互作用
接下来,研究人员发现,包括肺癌,乳腺癌,肝癌和卵巢癌以及黑色素瘤在内的多种癌细胞均可发生细胞焦亡,抑制磷酸化的Stat3可以有效的阻止PD-L1入核。另外,在缺氧条件下,在肿瘤细胞中nPD-L1将TNFα诱导的焦亡切换为焦磷酸化。
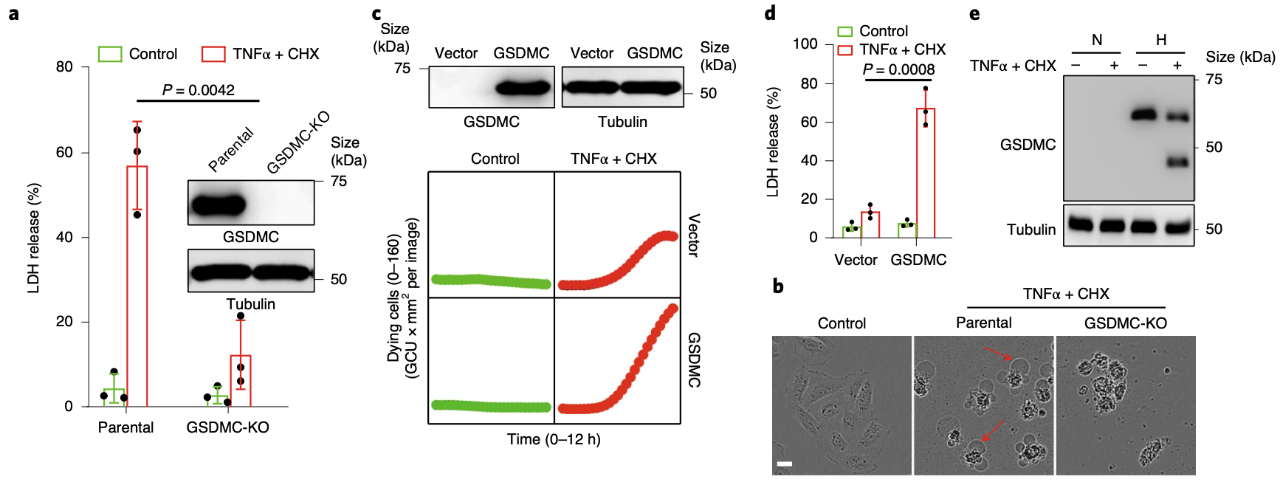
Caspase-8切割GSDMC诱导细胞焦亡
最后,体内实验显示,抑制核PD-L1介导的细胞焦亡通路可以显著缓解肿瘤坏死症状,并延长荷瘤小鼠的生存期。研究人员还发现抗生素类化疗药可诱导nPD-L1和GSDMC的表达以及caspase-8的激活,从而导致癌细胞的焦亡,影响PD-L1 +或GSDMC +癌症患者的抗肿瘤免疫力和预后。

GSDMC,nPD-L1和caspase-8是TNFα引起的缺氧区域肿瘤坏死所必需的
迄今为止,大多数PD-L1的研究都聚焦在其免疫检查点的功能。该研究首次阐明了肿瘤坏死需要nPD-L1、caspase-8和GSDMC的参与,揭示了与巨噬细胞焦亡截然不同的肿瘤细胞的焦亡通路。并提出抗生素类化疗药可在PD-L1 +或GSDMC +乳腺肿瘤的治疗中增强抗肿瘤免疫力,为后续的肿瘤治疗提供了重要参考。







