金秋九月,风爽天高雨后凉,凝露渐成霜。虽然国外仍处在疫情的阴霾下,但ESMO/CSCO两场享誉中外的肿瘤学会议还是顺利召开,药政、药企和科研人员与我们分享经验、洞悉前沿,更有多个极具影响力的临床数据公开。
PARP抑制剂作为肿瘤领域新药研发的热门方向,在近几年的全球医学大会上也展示了诸多突破性重磅研究结果,吸睛耀眼。比如,CSCO2018大会上,尼拉帕利对无论是否携带BRCA突变的卵巢癌患者均显现治疗效果;ESMO2019大会上,尼拉帕利再次登台,在卵巢癌一线维持治疗的研究中显著延长了PFS并降低疾病进展和死亡风险;ASCO2019/ESMO2019大会,奥拉帕利在去势抵抗前列腺癌中的临床数据公布,为PARP抑制剂的适应证拓展奠定基础;ESMO2020大会,除了国外的PARP抑制剂继续发力外,国内PARP抑制剂也开始彰显潜力,再鼎(尼拉帕利,已上市)、恒瑞(氟唑帕利,NDA)、百济神州(帕米帕利,NDA)、君实/英派(senaparib,临床III期)同台竞技。
PARP抑制剂:“合成致死”理念的成功运用,市场预测超100亿美元
PARP,即聚腺苷酸二磷酸核糖基聚合酶(poly ADP-ribose polymerase),是一类存在于真核细胞中催化聚 ADP 核糖基[poly(ADP-ribose),PAR]化的细胞核酶,属于一种关键的DNA修复酶,包括 PARP1、PARP2、PARP3等18个成员,在DNA损伤应答与修复、调控细胞凋亡、维持基因组稳定等方面具有重要作用。
PARP抑制剂是“合成致死”这一抗肿瘤理念运用于新药开发最成功的案例。合成致死(synthetic lethality)是指两个非致死基因同时被抑制,导致细胞死亡的现象。利用这一机制找到肿瘤中的特异突变,再找到它的“合成致死”搭档,进而特异性杀死癌细胞。PARP抑制剂是首个利用合成致死概念在临床上取得成功的药物。PARP抑制剂起效的关键因素是肿瘤细胞有同源重组修复缺陷(HRD),而BRCA蛋白是同源重组修复过程的重要蛋白,因此肿瘤细胞如果出现BRCA1/2基因突变,抑制PARP效果较好。
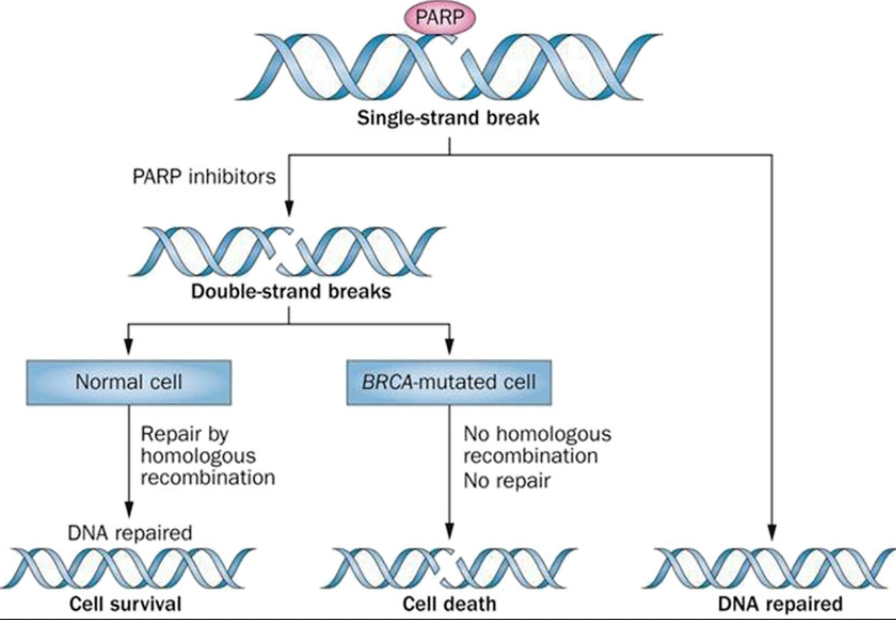
Nat Rev Clin Oncol. 2015 Jan;12(1):27-41
目前全球已上市PARP抑制剂有4个,分别是奥拉帕利(阿斯利康)、鲁卡帕利(Clovis)、尼拉帕利(GSK/Tesaro/再鼎)和他拉唑帕利(辉瑞),并且氟唑帕利(恒瑞)和帕米帕利(百济神州)也都向NMPA提交了上市申请。2019全球PARP抑制剂市场已经突破16亿美元,市场规模仍在快速增长,根据弗若斯特沙利文报告,预计至2030年,PARP 全球销售额有望突破123亿美元,中国市场销售额将达44亿元。
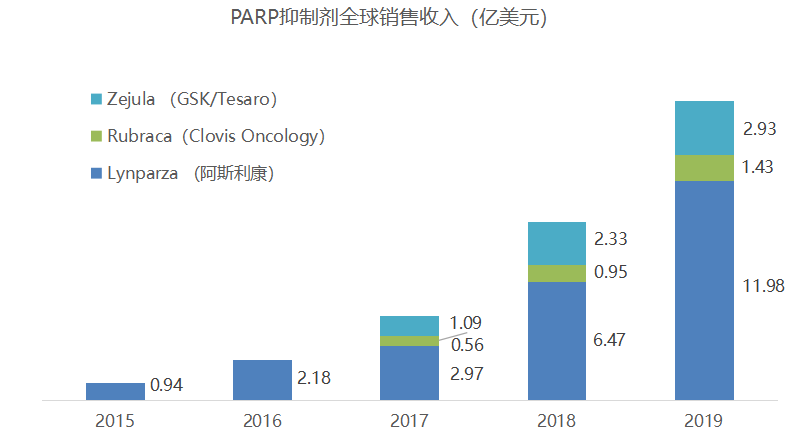
来源:公司财报、医药魔方
前景无限:覆盖多个瘤种,联合疗法的理想搭档
2014年,奥拉帕利获批的第一个适应症是用于三线及以上化疗后的BRCA突变的卵巢癌,正式宣告PARP抑制剂开发成功。时至今日,PARP抑制剂已经获批乳腺癌、胰腺癌、前列腺癌、卵巢癌、输卵管癌、腹膜癌等多个适应症,处于临床开发阶段的适应症还包括胃癌、非小细胞肺癌、结直肠癌、小细胞肺癌等,可以说PARP抑制剂覆盖了全球多个常见高发瘤种。
PARP抑制的潜力不单单表现在治疗领域广泛,更表现在对肿瘤治疗的深度影响上。ESMO 2020会议上,奥拉帕利公布一项SOLO-1研究的5年随访数据,显示奥拉帕利能够使BRCA突变的卵巢癌患者实现56个月的超长PFS,48.3%的患者5年疾病无进展,降低疾病进展或死亡风险67%。这一数据说明什么呢?说明采用奥拉帕利治疗的BRCA突变卵巢癌近一半的患者,在5年内疾病完全可控,肿瘤未显现恶化迹象,毫不夸张的说,这已经向“临床治愈”迈进了一大步。
正是由于出色的临床疗效,PARP抑制剂在临床指南中的用药推荐不断前移,从最初的三线以后治疗用药,到现在的多个一线用药资格,这些都在说明,PARP抑制剂对肿瘤治疗产生了重要而积极影响。
另外,随着临床使用范围的扩大,或者当肿瘤发生获得性耐药性后,PARP抑制剂与其他药物联用的治疗策略也再次显示出了可喜的治疗效果。在这一方面,PARPi也可与化疗、免疫治疗和靶向药物联合用药,希望通过协同效应和机制互补使药物产生更大治疗价值和效果。但受限于叠加的毒性,特别是PARP靶点固有的血液学毒性,尚无PARP与化疗的联合疗法获得成功。
在亮相本届ESMO大会的PARP抑制剂中,除了大家熟悉的奥拉帕利、尼拉帕利、氟唑帕利、帕米帕利之外,更让人感兴趣的是君实生物/英派药业联合开发的senaparib,因为在ESMO正式召开的1个月前,君实生物对外宣布与英派药业成立合资公司,向合资公司注资不超过3亿元,与英派药业合作在中国开发senaparib。君实生物为何愿意下注senaparib?这款药物有何竞争优势?可以带着问题看一下senaparib在ESMO大会上公布的数据。
senaparib:打造PARP抑制剂“安全性”新高地
Senaparib于2017年在中国和澳大利亚同步启动Ⅰ期临床研究,在中国的注册性II期和验证性III期研究已经分别于2019年11月和2020年1月完成首例患者给药。此次ESMO大会上公布的是Senaparib在中澳两地开展I期研究的最新数据。
I期研究主要评估senaparib的耐受性、安全性、PK和初步抗肿瘤活性。两项试验均采取标准3+3设计改良Fibonacci法,分为剂量递增和扩展两个队列。患者每日1次口服senaparib胶囊,3周为1个周期,直到疾病进展或出现不可耐受毒性。中国的临床研究中,在扩展阶段,除卵巢癌、输卵管癌和原发性腹膜癌外,患者需具备BRCA阳性突变。并且组织学或细胞学检查证实为至少经过一线系统性全身标准疗法治疗失败的难治恶性、晚期实体瘤,至少具备≥1个可评估或测量的病变(根据RECIST 1.1)。
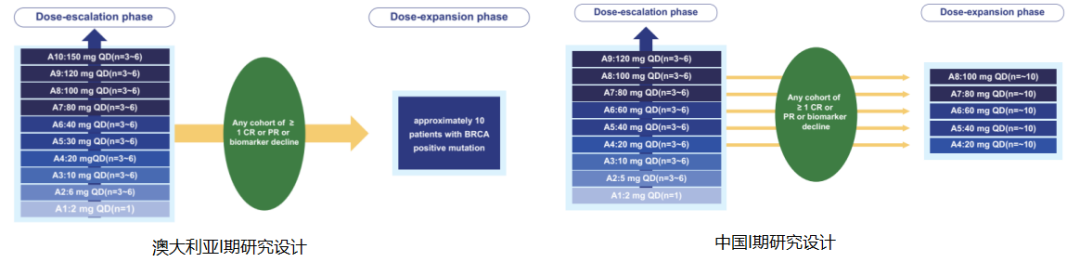
结果显示,senaparib具备潜在强大抗肿瘤效果。在澳大利亚的临床研究中,疾病控制率(DCR)达89.5%,17例可评估的BRCA+患者中有2例实现部分缓解,1例BRCA+卵巢癌患者的PR超过20个月,1例BRCA-前列腺癌患者PSA水平下降> 50%的时间持续了11个月。在中国的临床研究中,9例患者根据达到部分缓解(RECIST 1.1),ORR为22%,DCR为63.4%。其中6例患者为BRCA突变,故在BRCA突变患者(25例)中,senaparib的ORR为24%。同时,senaparib的暴露量随剂量递增(2mg-80mg)成比例增加,并且高剂量组呈饱和趋势(80mg,100mg和120mg)。基于毒性、药代动力学和疗效的综合分析,最终确定每日口服senaparib 100mg为II期推荐剂量(RP2D)。
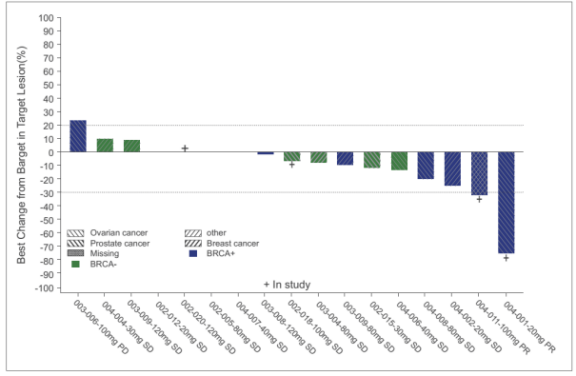
澳大利亚临床有效性数据
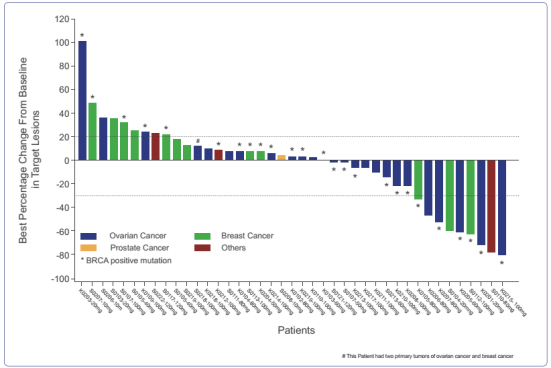
中国临床有效性数据
安全性方面,senaparib在两国患者中总体上可控且可耐受,皆未观察到剂量限制性毒性(DLT)。在中国患者中最常见的TRAE是白细胞计数下降(43.4%)、血小板计数下降(26.4%)、血红蛋白下降(24.5%)、贫血(24.5%)、食欲下降(24.5%)和乏力(24.5%)。大多数TRAE为1或2级,观察到17例≥3级TRAE和6例治疗相关的SAE,未观察到剂量限制性毒性(DLT)。整体来说,senaparib在澳大利亚和中国患者中均表现了初步的抗肿瘤活性和极佳的安全耐受性。
从I期数据来看,senaparib显示了初步的抗肿瘤效果,因为数据是在非最优剂量下获得的,senaparib的疗效潜力在后续临床研究中或可被进一步证实,而回归到“证明药物安全性和耐受性”的I期研究核心目的上面,senaparib是否又显示出了优势呢?
PARP抑制剂的不良反应大致相似但又各具特色,原因主要与不同PARP抑制剂的捕获能力、骨髓/血液浓度分布、脱靶作用等差异相关。2020年4月,在“第三届PARPi高峰论坛”上,黄萍教授等多位专家普遍认为,奥拉帕利无论是疗效与安全的平衡,抑或单纯的安全性问题,都不失为目前PARPi中最好的选择,那么,senaparib与奥拉帕利或其他PARP抑制剂相比是否具有更好的安全性?
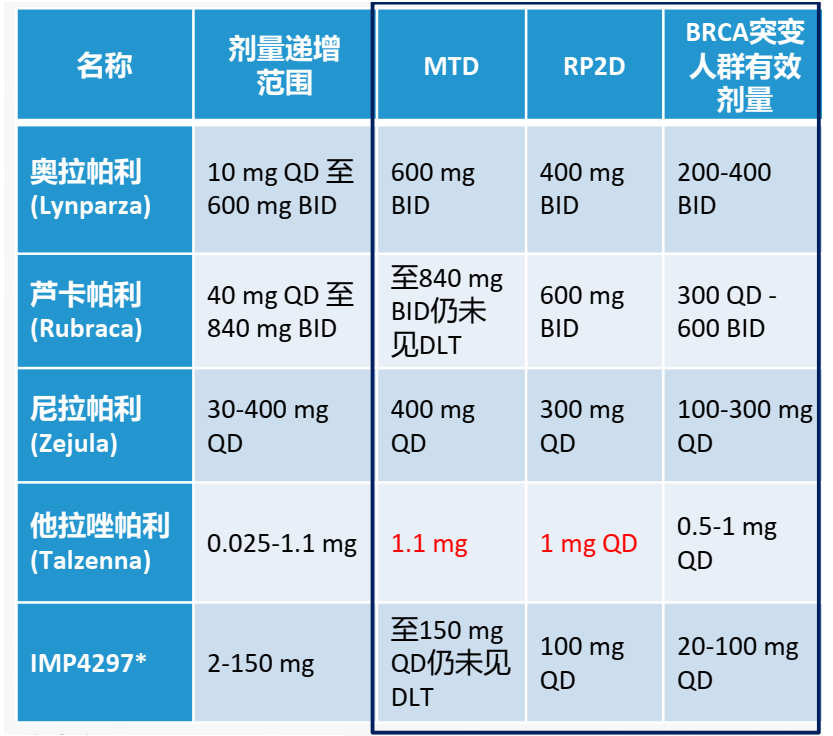
首先,senaparib在临床中展现了较高的活性和更宽的治疗窗口,与其他三种PARP抑制剂相比,senaparib的II期推荐给药剂量(RP2D)几乎是最低的,表明IMP4297对PARP的抑制活性较强,虽然他拉唑帕利的给药剂量最低(1mg),但已经接近其最大耐受剂量(1.1mg)。在上述披露的两个临床中,IMP4297最多给予了10个剂量(2mg-150mg)组递增,但在150mg仍未观察到剂量限制性毒性(DLT)。IMP4297在20mg便已经开始显现抗肿瘤活力,显示了7.5倍的治疗窗口,远高于其他PARP抑制剂,说明IMP4297在临床使用的剂量选择具有更大的灵活性。
其次,senaparib具有较高的PARP抑制活性,但并未增加相关血液性毒性。而在非血液毒性方面,包括恶心、便秘、呕吐、腹痛、腹泻等,几乎没有3级以上此类毒性,显示了优于其他PARP抑制剂的潜力。患者在治疗过程中,IMP4297发生药物剂量下调或停药的比例是15%和5%,是相对于上市药物中最低的数值。进一步证明,IMP4297具有良好的安全性和耐受性。
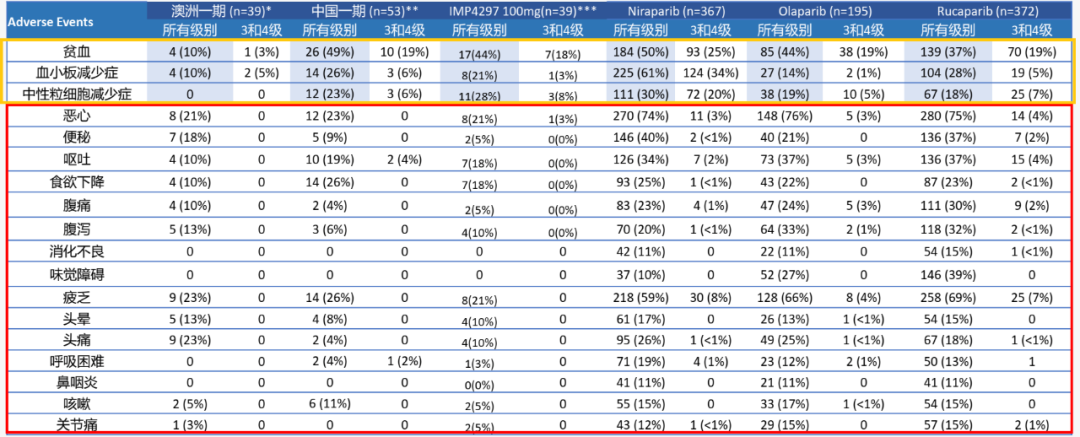
PARP抑制剂目前主要用于化疗后的维持治疗,肿瘤患者治疗之前的体质可能已经较差,在化疗之后体格更加发生变化,这就要求治疗药物在具有抗肿瘤作用的同时,应该具有较好的安全性和耐受性,在这一方面,senaparib已经具有优势。此外,正如奥拉帕利SOLO-1试验所证实的,患者存在可能的长期用药需求,因此药物良好的安全性和耐受性至关重要;同时,作为挖掘PARP治疗潜力的策略中,联合用药不失为一种首选的方案。senaparib所表现的较宽治疗选择窗口和安全性,无疑会对联合用药产生积极作用。据悉,英派已在海外启动senaparib与化疗药替莫唑胺(TMZ)联合治疗小细胞肺癌的临床1期研究,探索senaparib在联合用药方面的潜力。
总之,从目前披露的数据来看,Senaparib在安全性和耐受性方面表现卓越,甚至可以说具备同类最佳药物(best-in-class)的潜力。那么,Senaparib最终能否成为Best-in-Class药物呢?大家对其II期、III期疗效数据拭目以待吧。







