Kirsten鼠肉瘤病毒癌基因同源基因(KRAS)是人类癌症中最常见的突变癌基因,编码一种鸟苷三磷酸酶(GTPase),调节信号转导。据统计,约13%的非小细胞肺癌(NSCLC)和1%-3%的结直肠癌和其他癌症会发生RAS p.G12C突变。KRAS突变经常与靶向治疗的抵抗和癌症患者的预后不良有关。然而,目前仍没有被批准的选择性KRAS抑制剂。
Sotorasib是一种小分子药物,可特异性地且不可逆转地抑制KRASG12C。ERK是KRAS的一个关键下游效应因子,可持久抑制KRAS p.G12C肿瘤鼠肿瘤生长。临床前研究表明,Sotorasib可抑制细胞外信号调节激酶(ERK)的磷酸化。
近日,美国德克萨斯大学安德森癌症中心David S. Hong联合斯隆·凯特林纪念癌症中心Bob T. Li团队在《NEJM》杂志在线发表了题为“KRASG12C Inhibition with Sotorasib in Advanced Solid Tumors”的论文,研究了KRASG12C抑制剂Sotorasib治疗晚期实体瘤的疗效。

doi: 10.1056/NEJMoa1917239
针对KRAS p.G12C突变的晚期实体瘤患者,研究人员进行了一项关于sotorasib的1期临床试验。患者每日口服一次sotorasib。主要终点是安全性,关键次要终点是药代动力学和客观缓解。中位随访时间为11.7个月。
剂量递增和扩展队列研究共纳入129例患者,其中59例NSCLC患者、42例结直肠癌患和28例其他类型的癌症患者。107名患者(82.9%)停止治疗;停止治疗的最常见原因是疾病进展。截至2020年6月1日数据截止日,已有54名患者(41.9%)死亡。中位疗程为3.9个月(0~16.6个月)。治疗3个月以上74例(57.4%),6个月以上38例。
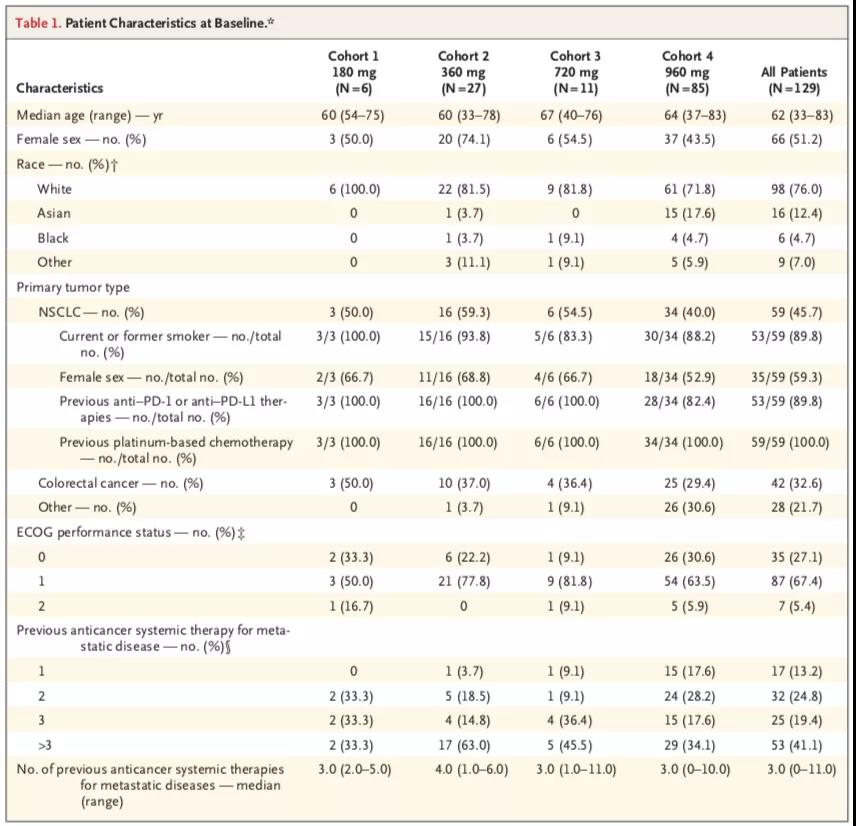
患者特征
安全性研究未观察到剂量限制性毒性作用,没有与治疗相关的不良事件导致死亡。125名患者(96.9%)发生了不良事件,最常见是腹泻(29.5%)、疲劳(23.3%)和恶心(20.9%)。共有73例患者(56.6%)发生治疗相关不良事件;15例患者(11.6%)在治疗过程中发生了3或4级不良事件。
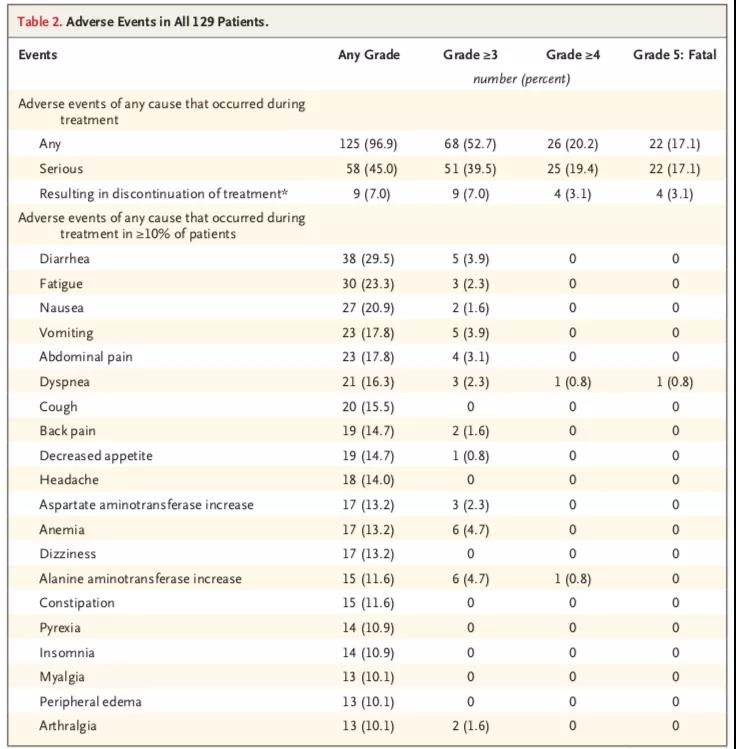
129例患者的不良事件
NSCLC亚组中,19例患者(32.2%)患者呈现完全或部分缓解,52例患者(88.1%)疾病控制(客观缓解或病情稳定),中位生存期为6.3个月。大肠癌亚组中,3例患者(7.1%)客观缓解,31例患者(73.8%)病情得到控制,中位生存期为4.0个月。胰腺癌、子宫内膜癌、阑尾癌和黑色素瘤患者病情也得到缓解。
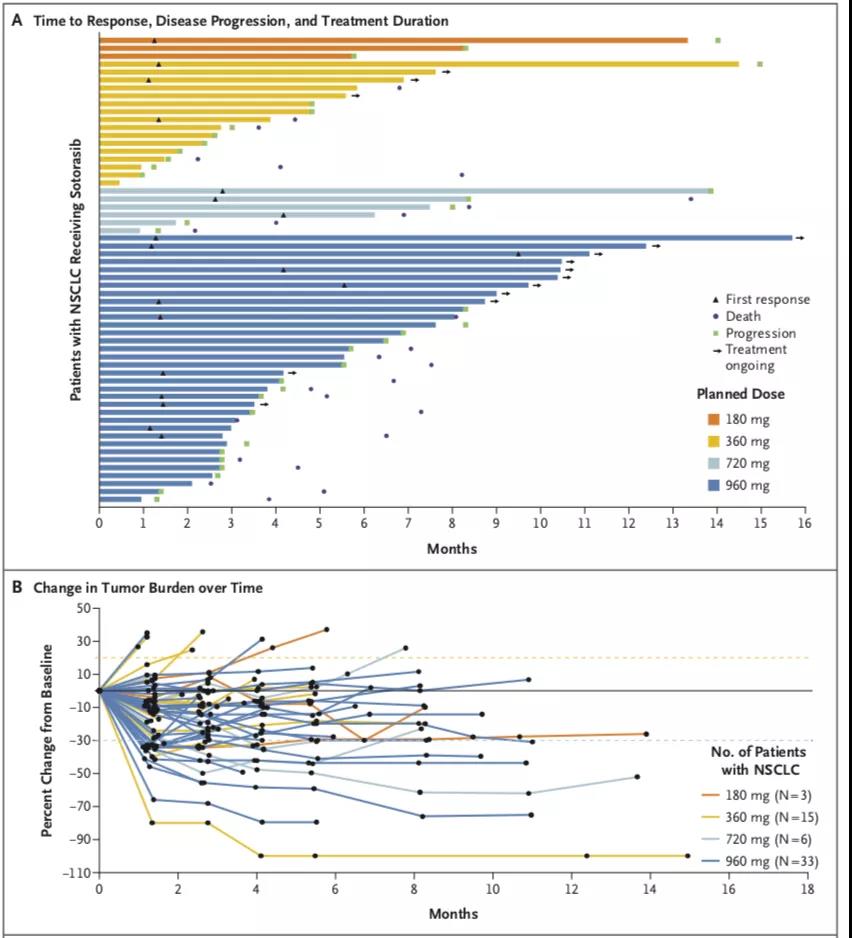
NSCLC亚组中Sotorasib的疗效
总之,Sotorasib对接受过治疗的KRAS p.G12C突变的晚期实体瘤患者显示出令人鼓舞的抗癌活性,但具有一定的毒副作用。评估Sotorasib单用或与多种药物联合治疗非小细胞肺癌或其他实体肿瘤患者的临床试验尚在进行中。







