10月26日,罗氏在中国提交的阿替利珠单抗(Tecentriq)第2项适应症上市申请进入“在审批”阶段,有望于近期正式获批,用于联合贝伐珠单抗治疗既往未接受过全身系统性治疗的不可切除肝细胞癌(HCC)患者。
HCC是一种治疗选择有限的侵袭程度很高的癌症,是全球癌症死亡的主要原因之一,约占肝癌90% 。全球每年有75万例新发肝细胞癌患者, 大多数病例来自亚洲,而几乎一半来自中国。据2015年中国肿瘤年报数据统计,中国每年有约37万例新发肝细胞癌患者,32.6万例患者因此失去生命。罗氏Tecentriq+贝伐珠单抗该适应症如果获批,将成为首个一线治疗HCC的免疫联合方案。
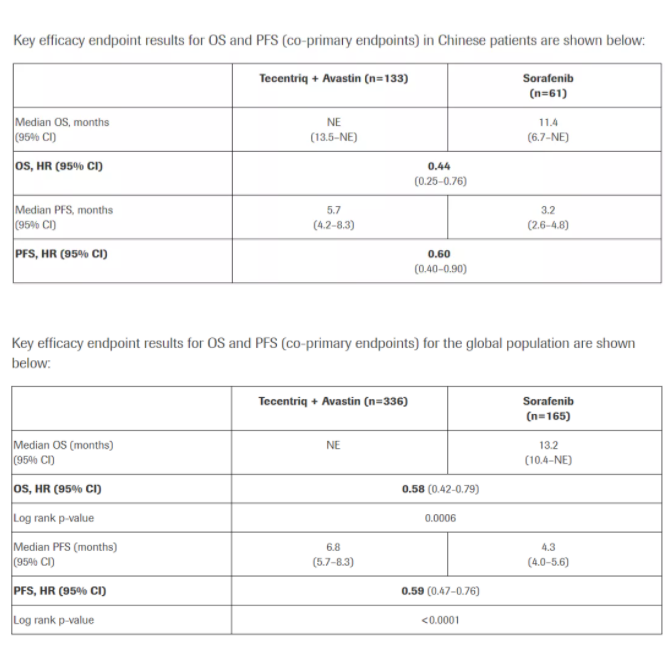
罗氏基于IMbrave 150研究中国队列数据向NMPA提交上市申请,该研究评估了Tecentriq+贝伐珠单抗 VS 索拉非尼一线治疗HCC患者的疗效和安全性,研究采用全球多中心、开放标签设计,501例既往未接受过系统性治疗的不可切除的HCC患者按照2:1分组。在纳入研究的194例中国患者(137例来自IMbrave150全球研究,57例来自中国扩展研究)中,133例患者随机接受Tecentriq+贝伐珠单抗治疗,61例接受索拉非尼治疗。
结果显示,Tecentriq+Avastin作为一线疗法相比索拉非尼显著延长了中国患者的总生存期(未成熟 vs 11.4个月),使死亡风险降低56%(HR = 0.44);同时显著延长了患者PFS(5.7 vs 3.2个月),疾病恶化风险降低40%(HR = 0.60)。该数据与IMbrave 150研究的全球数据一致。安全性方面,Tecentriq+贝伐珠单抗总体上耐受性良好,毒性可控,与已知数据一致。
罗氏Tecentriq于2020年2月在中国首次获批,用于治疗小细胞肺癌(SCLC)。此次一线肝癌适应症如果获批,将成为Tecentriq在中国获批的第2项适应症。另外,罗氏在中国提交的Tecentriq第3项适应症上市申请已经纳入优先审评,用于检测评估为≥50%肿瘤细胞PD-L1染色阳性(TC≥50%)或肿瘤浸润PD-L1阳性免疫细胞(IC)覆盖≥10%的肿瘤面积(IC≥10%)的表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非小细胞肺癌(NSCLC)患者的一线治疗。







