11月16日,Apellis公司宣布,FDA受理pegcetacoplan治疗阵发性睡眠性血红蛋白尿(PNH)的上市申请,并授予优先审评资格。PDUFA预定审批期限为2021年5月14日。
该项NDA申请是基于一项代号为PEGASUS的头对头III期临床研究。研究达到主要疗效终点:与依库珠单抗相比,pegcetacoplan治疗第16周时血红蛋白水平较基线的改善与对照组相比在统计学上有显著差异。数据还表明pegcetacoplan组溶血症状正常化率更高,慢性疾病治疗功能评估(FACIT)-疲劳评分也具有临床意义的改善。pegcetacoplan的安全性与依库珠单抗相当。
Pegcetacoplan是一种在研靶向补体C3疗法,旨在调节补体级联的过度激活,补体级联是人体免疫系统的一部分,过度激活可导致多种严重疾病的发生和进展。Pegcetacoplan是一种合成的环肽,与聚乙二醇聚合物偶联,特异性结合于C3和C3b。
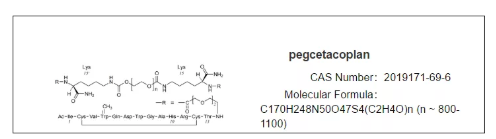
Pegcetacoplan结构

Pegcetacoplan目前正在开发的适应症和进展(来源:NextPharma)
依库珠单抗是Alexion公司开发的针对补体C5 的重组人源化单克隆抗体,于2007年首次获准上市,目前已获批4种罕见病适应症:PNH、非典型溶血尿毒症综合征(aHUS)、抗AchR抗体阳性全身性重症肌无力(gMG)、抗水通道蛋白-4(AQP4)抗体阳性的视神经脊髓炎谱系障碍(NMOSD)。依库珠单抗于2018年9月4日获NMPA批准上市,用于治疗成人和儿童PNH和非典型溶aHUS。依库珠单抗也是全球最畅销的孤儿药之一,2019年销售额高达39.46亿美元。
阵发性睡眠性血红蛋白尿症(PNH)是一种后天获得性溶血性疾病。该病源于造血干细胞PIG-A基因突变引起一组通过糖肌醇磷脂(glycosylphosphatidylinositol,GPI)锚连在细胞表面的膜蛋白的缺失,导致细胞性能发生变化。异常细胞缺乏GPI连接蛋白,从而对补体敏感,也因而引起相应的临床现象。血管内溶血、潜在的造血功能衰竭和血栓形成倾向是其3个主要临床表现。
PNH发病率在西方国家为(1~2)/100万人口/年,标化人口为1.3/100万人口/年。我国在2011年开始的全国9个中心的PNH登记研究中,截至2016年5月,共登记700例患者。PNH的发病率至今没有非常精确的统计,但总的来说,北方比南方更为常见,总的发病率应与再生障碍性贫血(再障,AA)类似,在1/10万左右,较欧美常见。发病年龄在各年龄组均有报道,从2岁至80岁以上,但无论国内外均以青壮年患者居多,20~40岁约占77%。男女均可发病。北京协和医院报道,中国与其他亚洲国家患者女性比例相似,均显著低于欧美国家。综合国内14个不同地区报道的651例中男女之比2.4:1。
Apellis公司首席医学官FedericoGrossi博士说,十多年来,C5抑制剂是治疗PNH的唯一选择,许多患者仍在遭受持续的低血红蛋白困扰,需经常忍受衰弱性疲劳和频繁输血。FDA授予的优先审评资格使pegcetacoplan距离有需要的患者更近了一步。研究数据证明了靶向补体C3的治疗潜力,我们将继续推进该靶点针对很少或根本没有治疗方法的严重疾病的多项注册研究。







