1月29日,国办发[2021]2号文公布,预示着带量采购成为一项常态化、制度化的工作,板上钉钉。
文件下发当日,国新办举行新闻发布会,医保、药监、卫健等部门的相关负责人介绍了2号文的基本情况并回答了记者提问。在回答记者提出具体哪些药物能够进入集采目录,标准是什么的问题时,国家医保局副局长陈金甫说:“能否触发国家组织集采是有严格的规则设置,基本上是采取原研药加通过一致性评价的仿制药,只要达到三家就可以列入集采”。“选择的条件重点是医保目录内、临床必须、用药量大、金额高,形成了集采触发机制。这种做法既保证质量要求,也保证企业公平竞争的客观条件,也符合临床要求,更避免竞争规则的自由裁量权。”生物类似药纳入集采“毫无疑义”,包括中药大品种纳入集采是制度性的要求
对于生物药纳入集采的问题,有记者认为生物类似药与化学仿制药的质量把控标准不同,化学仿制药的一致性评价是无法完全平移到生物类似药的评判过程中,该记者提出,这会给未来生物药带量采购的真正落地带来哪些影响?他指出,“生物类似药跟化药的仿制药质量评价方式上有差别,但是它有严格的质量标准,下一步纳入集采是毫无疑义的。一些地方进行了探索,并且中选产品质量是完全可控的”。“所以按照国办发2号文件以及探索的情况来看,生物类似药纳入集采,包括中成药的大品种纳入集采,这是制度性的要求,只不过规则更为优化,更有针对性,质量更符合药本身的属性,从我们国家来说,生物类似药质量标准全球还是比较高的,高于西方一些国家”。陈金甫归结为两句话,一是纳入集采是毫无疑义的;二是质量一定是作为我们优先的考量,规则一定更符合市场要求。据悉,2019年我国首个生物类似由复宏汉霖研发上市后,相继有利妥昔单抗、阿达木单抗、贝伐珠单抗、曲妥珠单抗的生物类似药获批上市。涉及的厂家包括复宏汉霖、海正药业、百奥泰、齐鲁、信达生物等。其中,利妥昔单抗、阿达木单抗、贝发珠单抗已经满足3家及以上数量,达到集采的条件。除此之外,其他生物类似药也在不断上市路上或在临床阶段,如下图:
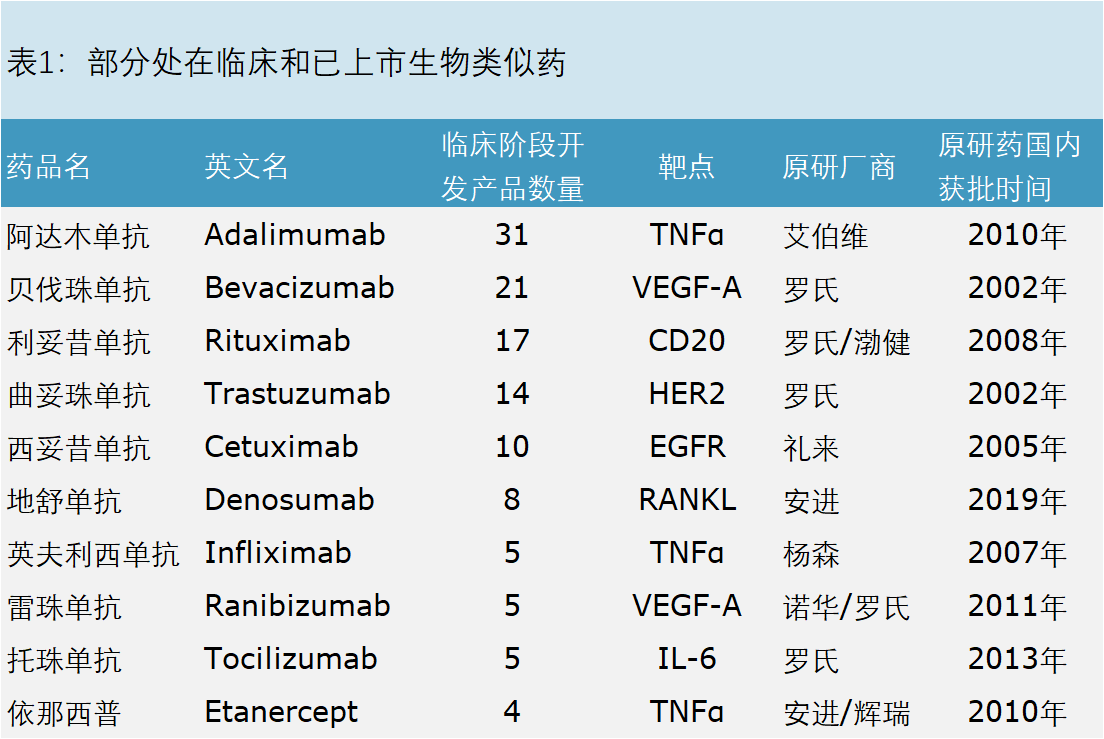
前三批国家组织药品集采共涉及112个品种,中选产品的平均降幅达到了54%,截至2020年,实际采购量已经达到协议采购量的2.4倍,节约费用总体上超过了1000亿元。同时,地方按照国家组织集中采购的基本规则,开展药品集中带量采购工作,省级集采累计达到259个品种,每年可节约费用达到240亿元。第四批集采即将于2月3日在上海开标,有45个品种纳入集采目录,请持续关注集采相关话题。

