中药注射剂,淘汰赛开始。
01 一中药注射剂被召回停用
1月11日,国家药监局发布《关于注销莲必治注射液药品注册证书的公告(2022年第2号)》,宣布即日起停止莲必治注射液在国内的生产、销售、使用,并注销其药品注册证书。

公告要求,已上市销售的产品,由药品上市许可持有人负责召回,召回产品由所在地省级药品监督管理部门监督销毁或者依法采取其他无害化处理等措施。
资料显示,莲必治注射液主要成分为亚硫酸氢钠穿心莲内酯,主要用于细菌性痢疾,肺炎,急性扁桃体炎。
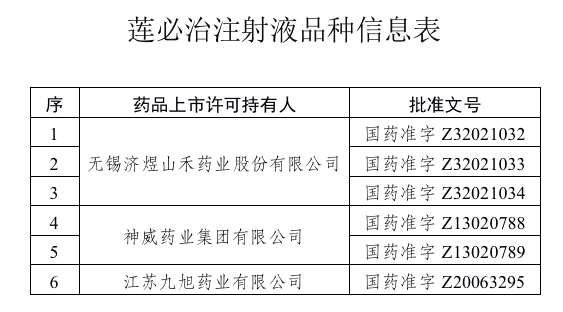
据国家药监局数据,目前国内拥有莲必治注射液批文的厂家有三家,分别是无锡济煜山禾药业股份有限公司、神威药业集团有限公司、江苏九旭药业有限公司。
02 安全性问题被高度重视
虽然国家药监局对作出以上决定的原因未做说明,但在公告中提到,“根据《中华人民共和国药品管理法》第八十三条等有关规定,国家药品监督管理局组织对莲必治注射液开展了上市后评价”,本次公布的决定也是经评价后的结果。
根据《中华人民共和国药品管理法》第八十三条,药品上市许可持有人应当对已上市药品的安全性、有效性和质量可控性定期开展上市后评价。必要时,国务院药品监督管理部门可以责令药品上市许可持有人开展上市后评价或者直接组织开展上市后评价。
从这一点看,本次国家药监局注销莲必治注射液的批文,主要与其安全性、有效性和质量可控性有关。事实上,一直以来中药注射剂的有效性、安全性问题就饱受争议。
说到中药注射剂的安全问题,要追溯到2006年的“鱼腥草注射液事件”。
当时,由于鱼腥草注射液导致的严重不良反应甚至死亡事件频发,国家药监局发布暂停使用鱼腥草等7个注射剂的通告。自从“鱼腥草注射液事件”后,人们对中药注射剂安全性等方面提出了质疑。
对于中药注射剂,冀连梅药师曾发文表示,注射液中出现热原的主要原因是原料带入。因中药注射剂的原料是各种草药,来源复杂,而中药注射液又不要求纯化到单一成分,因此中药注射液容易产生热原,这是中药注射液先天的缺陷。
近年来,国家药监部门越来越重视中药注射剂的安全性问题。
以莲必治注射液为例,早在2006年,原国家食药监局就曾要求其修订说明书,明确老年人、儿童、孕妇、哺乳期妇女及有肾脏疾病的患者应慎用。
2018年儿童节前夕,国家药监局发布公告,作为在临床已应用70多年的中药注射剂、儿科的常用药的柴胡注射液,因为不良反应等原因,从此被禁用于儿童。
同年,人们熟悉的双黄连注射液也被要求增加警示语“本品不良反应包括过敏性休克”,同时要求4周岁及以下儿童禁用。
03 医疗机构限制使用
众所周知,在2021版医保目录中,有40个中药注射剂被限二级以上医疗机构使用。具体如下:

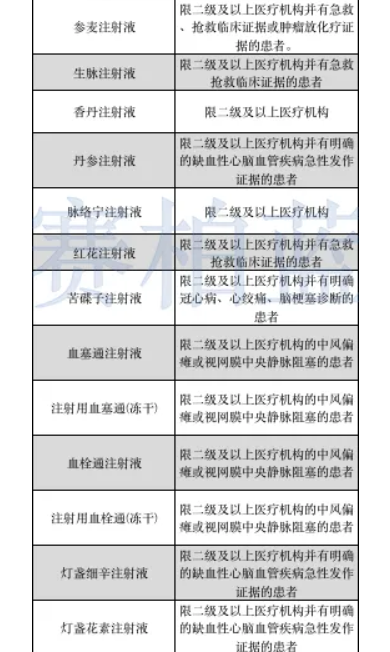
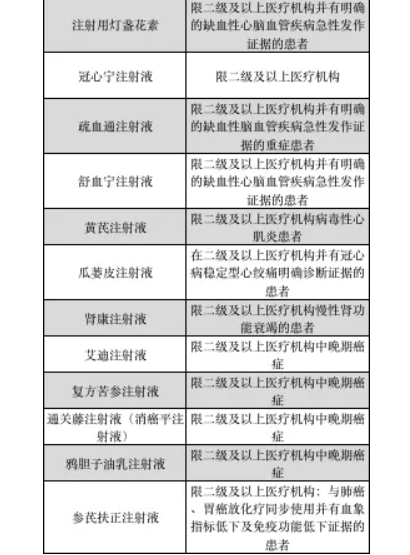
说到限制使用,也是动真格的。近日,江西遂川县辖下的20家乡镇卫生院因违规使用血栓通注射液、醒脑静注射液、生脉注射液、参麦注射液、香丹注射液、清开灵注射液等多种中药注射液,被当地医保局责令限期整改,并累计追回违规补偿款约87万元,违规金额0.3万至9万多元不等。
随着国家监管部门对中药注射剂的重点关注,除了被限制使用以及修订说明书,还有重点监控目录、药品集采,从国家到地方,对于中药注射剂的监管越来越严格。
不过,值得一提的是,中药注射剂也具有起效快、疗效好等优势,对某些疑难重症、危急重病的治疗效果较好。在新冠疫情期间,就有多款中药注射剂被广泛使用,并纳入诊疗指南。
在严格的监管下,中药注射剂安全性逐渐提高,也是不争的事实。
据《2020年度国家药品不良反应监测年度报告》,在注射剂(不含疫苗)总体报告中,中药注射剂占7.8%;注射剂(不含疫苗)严重报告中,中药注射剂占6.1%。同时,在临床发生不良反应的药品中,中药占13.4%,近5年保持整体下降趋势。
随着中药注射液上市后再评价的开展,中药注射剂迈进高质量发展的新赛道。能够留下来的一定是疗效确切、安全性高的品种,而对于那些存在缺陷的品种,莲必治注射液就是一道缩影,淘汰是必然的结局。







