近日,中国国家药品监督管理局(NMPA)正式受理普拉替尼(Pralsetinib)胶囊的上市申请并纳入优先审评,用于治疗经含铂化疗的RET融合阳性的非小细胞肺癌(NSCLC)患者。
普拉替尼是由基石药业战略合作伙伴Blueprint Medicines Corporation开发的一款口服、高选择性强效RET(rearranged during transfection)单一靶点抑制剂,每日一次,服用方便,具有较好的依从性。基石药业拥有普拉替尼单药或联合治疗在大中华地区(包括中国大陆、香港、澳门和台湾地区)的独家临床开发与商业化权利。在大中华地区外,Blueprint Medicines Corporation与罗氏/基因泰克达成全球合作。罗氏拥有普拉替尼在大中华区(包括中国大陆、香港、澳门和台湾地区)和美国以外市场的全球独家许可,以及在美国和Blueprint Medicines Corporation共同开发和商业化普拉替尼的权利。
9月4日,普拉替尼刚刚获得FDA批准,用于治疗RET融合阳性的局部晚期或转移性NSCLC成人患者。FDA批准普拉替尼主要基于关键I/II期ARROW研究的数据。ARROW研究旨在评估普拉替尼对RET融合阳性NSCLC、甲状腺癌以及其它携带RET变异的晚期实体瘤的安全性、耐受性和疗效。在87例既往接受过含铂化疗的患者中,普拉替尼治疗组患者的ORR为57%,CR 5.7%。在27例不适合接受含铂化疗的初治患者中,ORR为70%,完全缓解率为11%。
基石药业在中国开展的注册桥接试验于2019年8月实现首例经含铂化疗的RET融合阳性的NSCLC患者给药,同年12月完成了最后一例患者的入组。结果显示普拉替尼在既往接受过含铂化疗的RET融合阳性NSCLC患者中显示出了优越和持久的抗肿瘤活性,并且安全性及耐受性良好,数据与ARROW研究的全球患者人群一致。基石计划将在未来的学术会议上发布ARROW研究RET融合阳性的NSCLC中国患者的数据结果。从7月份全球I/II期ARROW关键性试验的中国患者研究结果数据发表到在中国递交NDA,基石药业只用了两个月时间。
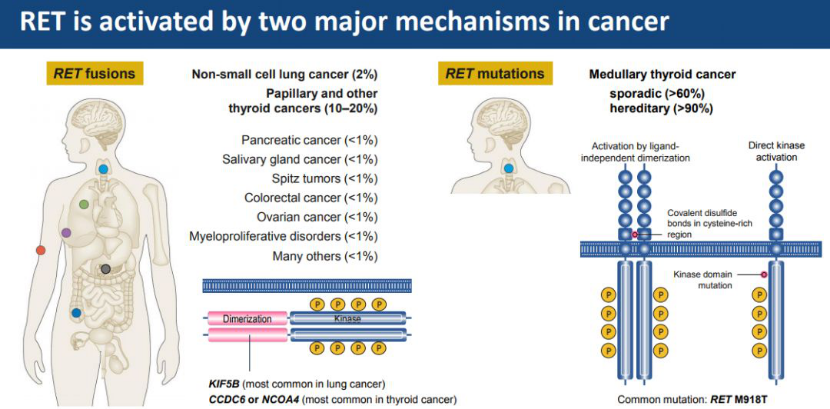
RET融合阳性癌症和RET突变阳性甲状腺髓样癌的肿瘤细胞分化和增殖高度依赖于RET蛋白的激活,这种依赖性通常也被称为“致癌基因成瘾”,因此RET阳性肿瘤对高选择型的单靶点RET抑制剂非常敏感。RET基因融合在NSCLC患者中的发生率约为1%~2%,在甲状腺乳头状癌(占所有甲状腺癌的85%左右)中的发生率为10%~20%。RET基因突变在甲状腺髓样癌中的发生率为60%左右。
目前对于RET融合突变肿瘤的治疗方案主要是使用多激酶抑制剂类药物,比如卡博替尼、凡德他尼,由于靶向选择性不高,疗效非常有限且毒性较大。普拉提尼不仅可以为RET阳性实体瘤患者带来强劲而稳定的疗效,而且3级以上不良事件发生率低,生存获益非常显著。普拉替尼也曾被FDA授予治疗经含铂化疗后进展的RET融合NSCLC以及需要系统治疗且没有可替代治疗方案的RET突变阳性甲状腺髓样癌的突破性疗法资格。
ARROW研究主要研究者,广东省人民医院吴一龙教授表示:“在肺癌精准治疗领域,针对RET靶点的研发是继EGFR、ALK、ROS1和NTRK等靶点后另一个巨大的突破。目前,国内尚无选择性RET抑制剂获批。对于RET融合阳性NSCLC患者,国内尚存在巨大未满足的临床治疗需求。普拉替尼在全球性试验以及在中国NSCLC患者中的研究结果令我们对其在国内的上市及其对患者带来的获益充满期待。”
基石药业董事长兼首席执行官江宁军博士表示:“我们很高兴看到NMPA已受理普拉替尼用于治疗经含铂化疗的RET融合阳性NSCLC的适应症上市申请,并将其纳入优先审评。这是基石药业今年在全球递交的第3个、中国大陆递交的第2个新药上市申请,充分表明了基石药业正在商业化战略转型的道路上加速迈进。我们期待普拉替尼早日在国内上市,为中国广大RET融合阳性NSCLC患者带来新的治疗希望。”
基石药业首席医学官杨建新博士表示:“我们很高兴看到普拉替尼在临床试验中展现了快速和持久的抗肿瘤活性以及良好的安全性及耐受性。值得一提的是,从我们与Blueprint Medicines Corporation达成合作到普拉替尼在国内成功递交上市申请仅用了2年时间。我们将继续全力推进普拉替尼在中国的研发进展,更广泛地评估该产品在未经含铂化疗的RET融合阳性的NSCLC、甲状腺髓样癌和其它实体瘤患者中的疗效,早日满足这部分癌症患者亟待解决的临床需求。“







