今日,GemVax & KAEL公司(下称GemVax)宣布,该公司在研疗法GV1001治疗阿尔茨海默病患者的积极2期临床试验结果在Alzheimer's Research & Therapy杂志上发布。GV1001是一种端粒酶调节剂。基于积极的2期临床结果,GemVax计划在今年晚些时候在韩国进行3期临床试验。

阿尔茨海默病(AD)是老年人最常见的神经退行性疾病,在2019年全球有超过3500万患者,其中绝大多数是60岁以上的老人。AD不但剥夺了他们的记忆,还严重影响他们的认知和生活自理能力,不但对患者个体,而且对他们的家人、社区和国家都产生深远的负面影响。然而,在AD疗法开发领域, 2003年至今,美国FDA尚未批准任何治疗AD的创新药。
GV1001是一种由16个氨基酸组成的多肽,它对应人类端粒酶逆转录酶(TERT)的催化位点片段。TERT是端粒酶的重要组成部分,对调节端粒酶的活性非常重要。此前的研究显示GV1001能够防止神经细胞免受神经毒性的影响,防止细胞凋亡以及由于淀粉样蛋白和氧化应激产生的活性氧对神经细胞的损害。因此,GemVax的科学家们认为它可能成为治疗阿尔茨海默病的一种选择。
在随机双盲,含安慰剂对照的2期临床试验中,总计96名阿尔茨海默病患者接受了安慰剂或不同剂量的GV1001的治疗。试验的主要终点是使用称为SIB(severe impairment battery)的评分系统对患者的评估。
试验结果显示,在接受治疗24周之后,接受较高剂量GV1001治疗的患者的SIB评分与安慰剂组相比得到显著改善。这一改善在接受治疗12周之后也可以观察到。在安全性方面,GV1001的安全性与生理盐水相同。
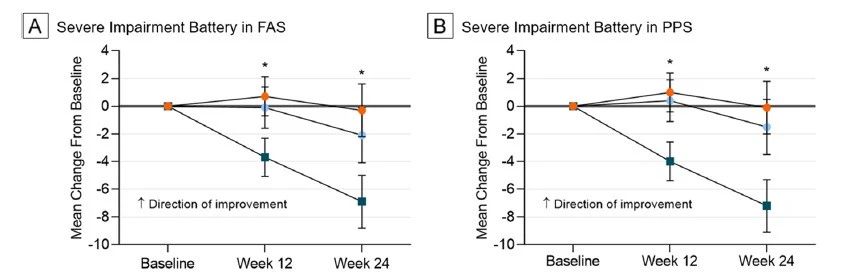
▲接受不同剂量GV1001或安慰剂治疗的患者的SIB评分变化,橘色为最高剂量GV1001治疗组,深蓝色为对照组(图片来源:参考资料[2])
GemVax已经向韩国监管机构递交IND申请,寻求启动3期临床试验检验GV1001的疗效。同时,该公司也已经获得FDA的批准在美国进行2期临床试验,治疗轻度阿尔茨海默病患者。







